- 2021/07/26 掲載
富士通、製薬・医療機器メーカー向けSaaS型治験ソリューションを提供開始
「DDworks NX」は、医療機関、製薬、医療機器メーカーで行う治験業務の各段階において、従来、紙媒体でやり取りが行われていた治験文書をデジタル化するとともに、2019年1月に提供開始した医療機関向けSaaS型ソリューション「tsClinical DDworks21/Trial Site(トライアル サイト)」(以下、「Trial Site」)と連携することで、医療機関と、製薬、医療機器メーカー間での治験文書のデジタル連携を実現します。これにより、製薬、医療機器メーカー双方の治験業務を効率化し、人件費や書類の外部保管倉庫にかかるコストの削減、治験従事者の働き方改革に貢献します。さらに、利用画面の日本語、英語切り替え機能の追加で、増加する国際共同治験(注1)への対応や翻訳作業の負荷を軽減するほか、対応ブラウザの追加でユーザーエクスペリエンスを向上させます。
当社は、今後も治験業務プロセスのデジタル化によりさらなる効率化を実現し、患者へ新しい医薬がより早く届くことを通じて、あらゆる人のウェルビーイングの向上への貢献を目指します。
■背景
一つの新薬を開発するためには、一般的に約15年の期間と数百億円から1千億円以上の研究開発費(注2)がかかると言われています。その中でも、新薬開発における医療機関および製薬メーカーや医療機器メーカーとの治験文書の手続きや、照合と検証を意味するSDV(注3)などのやり取りの大半が、製薬、医療機器メーカーの担当者による紙媒体を使った直接訪問、原紙保管で進められ、多大な労力とコストを要していることが課題となっています。
また、近年コロナ禍において、直接訪問には制約があるため、これらの業務のデジタル対応への要望が急速に高まっていました。
さらに、国際共同治験比率の上昇や海外ステークホルダーとのClinical CAPA(注4)の実践などに伴う、治験文書管理システムのグローバル対応も求められていました。
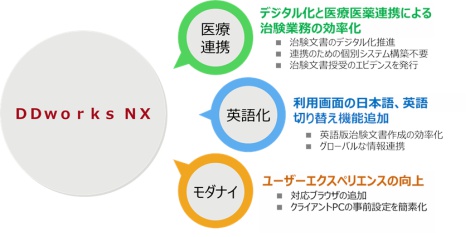
■「DDworks NX」の主な特長
1. デジタル化と医療連携による治験業務の効率化
「DDworks NX」は、医療機関が利用する「Trial Site」とシームレスに連携することで、医療機関と製薬、医療機器メーカーそれぞれで管理を行うISF(注5)をはじめとする治験に関する文書をリアルタイムで確認可能とする仕組みを提供します。また「DDworks NX」および「Trial Site」それぞれにおいて治験文書のやり取りをしたエビデンスを発行することも可能です。これにより、従来、製薬、医療機器メーカーの担当者が医療機関へ直接訪問して行っていた紙媒体での治験文書に関する業務がデジタル上で完結することとなり、人件費や書類管理のコストの削減、治験従事者の働き方改革に貢献します。
なお、「DDworks NX」は、製薬、医療機器メーカーと医療機関が連携するための機能を標準実装していることから、個別システム構築は一切不要なため、システム構築、運用面でのコスト削減にも寄与します。
2. 利用画面の日本語、英語切り替え機能追加
「DDworks21」にはなかった英語版の利用画面を追加したことにより、治験文書の記載項目の英訳が不要になります。これにより、FDA(注6)などへの査察対応における英語版の治験文書作成を効率化します。また、グローバルでのClinical CAPA実践など国際共同治験における情報連携を容易にし、治験業務の品質向上に貢献します。
3. ユーザーエクスペリエンスの向上
EdgeやChromeなどのブラウザへ対応したWebデザインに刷新することで操作性などのアクセシビリティを向上したほか、専用ビューアーでのみ参照可能だった帳票のPDF化により、情報の保存性、汎用性も向上しました。また、最大20箇所以上の設定が必要だったクライアントPCにおける複雑な事前設定を一箇所に簡素化することで、利用者の追加やクライアントPC入替時に発生していたトラブルの抑止など、システム管理者の負荷も軽減します。
注1 国際共同治験:複数の国や地域で同時に行われる治験。
注2 一般的に約15年の期間と数百億円から1千億円以上の研究開発費:出典 第1回医薬品開発協議会 2020年10月27日 日本製薬工業協会
注3 SDV:Source Document Verificationの略、原資料の照合と検証。
注4 Clinical CAPA:Clinical Corrective Action and Preventive Actionの略、臨床試験における是正、予防措置。
注5 ISF:Investigator Study Fileの略、医療機関で保管する治験の実施及びデータの品質に関する文書。
注6 FDA:Food and Drug Administrationの略、アメリカ食品医薬品局。
PR
PR
PR